/i.s3.glbimg.com/v1/AUTH_59edd422c0c84a879bd37670ae4f538a/internal_photos/bs/2020/F/k/tBFGEbS8atYvjkrmafUA/063-1264549603.jpg) Amostras de sangue de pacientes são vistas em um teste de vacinas contra a Covid-19 na Flórida no dia 7 de agosto. — Foto: Joe Raedle/Getty Images/AFP
Amostras de sangue de pacientes são vistas em um teste de vacinas contra a Covid-19 na Flórida no dia 7 de agosto. — Foto: Joe Raedle/Getty Images/AFP
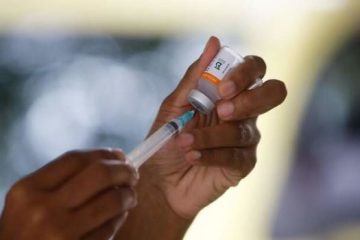
Amostras de sangue de pacientes são vistas em um teste de vacinas contra a Covid-19 na Flórida no dia 7 de agosto. — Foto: Joe Raedle/Getty Images/AFP
A vacina BNT162b1, uma das candidatas contra a Covid-19 das farmacêuticas BioNTech e Pfizer, induziu uma resposta imune “robusta” e não teve efeitos colaterais graves em voluntários adultos, mostram resultados preliminares publicados nesta quarta-feira (12) na revista científica “Nature”, uma das mais importantes do mundo.
A resposta imune aumentou conforme a dose aplicada, e também foi maior com uma segunda dose da vacina, de reforço.
A BNT162b1 foi bem tolerada, embora alguns participantes tenham apresentado efeitos colaterais leves a moderados, que aumentaram com o nível da dose, nos sete dias após a vacinação, incluindo dor no local da injeção, fadiga, dor de cabeça, febre e distúrbios do sono, mostra o estudo.
Os resultados divulgados foram os das fases 1 e 2, que testam a segurança e a eficácia de uma vacina, respectivamente. As etapas ainda estão em andamento.
A imunização também está sendo testada no Brasil – em São Paulo e na Bahia.

Pfizer inicia teste de vacina com voluntários no Brasil
Resultados
Houve 45 participantes nos testes (23 homens e 22 mulheres), divididos em 4 grupos:
- Um grupo recebeu uma dose de 10 microgramas (μg) da vacina;
- Outro grupo recebeu uma dose de 30 microgramas (μg);
- O terceiro recebeu 100 microgramas (μg);
- O quarto recebeu um placebo (substância sem a vacina, para servir de grupo controle).
Os participantes que receberam 10 ou 30 microgramas também tomaram uma segunda dose da vacina, aplicada 21 dias depois da primeira.